高校理論化学:【偏差値70超えの暗記ノート】
執筆中です。


理論化学の中でも溶解平衡は難しくなる傾向があります。
▶ 結晶格子の問題
結晶の問題は面倒くさい計算中心になります。計算時は大きめに書いてケアレスミスを防ぎましょう。
・密度の計算、充填率の計算、限界イオン半径比が出ます

密度の計算は必ずミスなく!

充填率は単位格子の体積に含まれる原子の体積の割合のこと。六方最密構造が一番苦手に感じる人が多そう。

限界半径比は、結晶構造がほぼ安定しているときの陽イオン半径/陰イオン半径の計算結果のこと。塩化ナトリウム型と塩化セシウム型は暗記してました。
| 塩化ナトリウム型結晶 | 塩化セシウム型結晶 | |
|---|---|---|
| 限界イオン半径比 | √2ー1 | √3ー1 |
・体心立方格子
| 配位数 | 単位格子中に含まれる原子の数 | |
|---|---|---|
| 8 | 2つ |
・面心立方格子
| 配位数 | 単位格子中に含まれる原子の数 | |
|---|---|---|
| 12 | 4 |
・六方細密構造

みんながつまずきやすいところはおそらく、①充填率を求める際に使う単位格子中の原子の数(2)、②体積を求める際に使う三角錐の計算です。
| 配位数 | 単位格子中に含まれる原子の数 | |
|---|---|---|
| 12 | 2 |
・塩化ナトリウム型のイオン結晶

イオン結晶は塩化ナトリウム型と塩化セシウム型の2つがよく出ます。
・塩化セシウム型のイオン結晶
・共有結合型の(ダイヤモンド型)結晶

難関大は共有結合型の結晶格子の計算をよくさせる印象
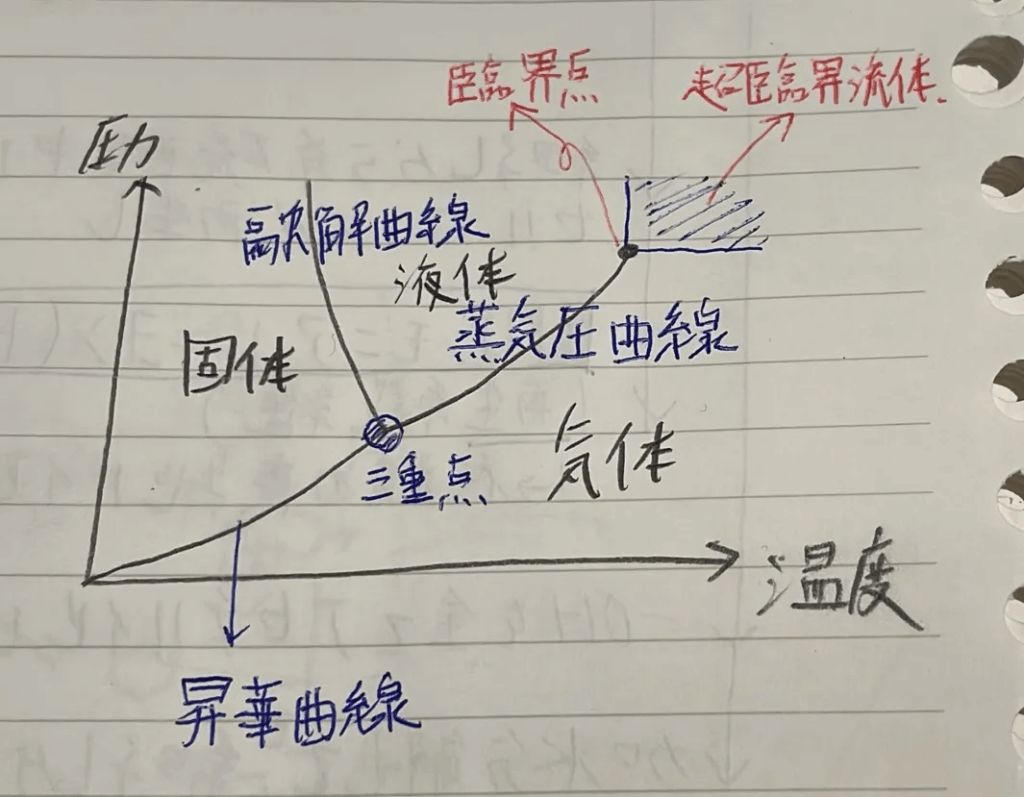
▶ 純物質の状態変化の問題

当サイトのコンテンツはすべて無料で閲覧できます!以下の作業用勉強タイマーで読者の勉強時間を最大効率化させるお手伝いもできたら嬉しいです!

▶ 化学平衡の問題
▶ 【難】電離平衡・溶解平衡の問題

近似計算は、難関大では誘導されない場合が多いです。一般的には、電離度を求めた時、電離度が0.05を超えるようであれば、電離度に関する二次方程式を解きます。
・ 電離定数が極端に小さい時、電離を無視できる
酢酸(CH₃COOH)は水に溶けると、一部だけが電離して

となります。このときの平衡定数(電離定数)は
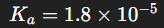
と非常に小さく、ほとんどの酢酸分子は電離していないということを意味します。
たとえば 0.1 mol/L の酢酸水溶液を考えると、電離して生じる H⁺ の濃度は約 0.0013 mol/L。
元の濃度 0.1 mol/L に比べて非常に小さいので、計算のときは「0.1 − α ≈ 0.1」として電離を無視してもほとんど誤差が出ません。
・ 温度不変で平衡定数は不変
小門集合の時、1番で求めた平衡定数をのちの温度が同じ実験で使ったりします。この事実を覚えて、平衡どうやって求めるんだ、、、ってならないようにしましょう。
▶ 理想気体と実在気体分圧計算の問題など
・ 条件付きで、高温または低圧にするとZが1に近づく


アンモニアなどは分子間で水素結合をし、分子間力の影響が大きいです。なので極性がなかったり分子間力が弱いものよりもVが小さくなり、Zが小さくなります。
▶ ヘンリーの法則を使う問題
・ ヘンリーの法則


体積について考察する際も、その体積分の空間を想定してmolで考察すると楽です。ヘンリーの問題で困ったらmolに変換して考えましょう。
・ ヘンリーの法則の問題で困ったらmolに直して考えてみる


上記のように、気体にn2モル溶けた状態を考えると、n1とn2を足した値は常に同じです。また、気体定数が与えられていなくても、Rとおいて計算すればうまく消えてくれる場合がほとんどです。
▶ エネルギー収支(熱化学・エンタルピー変化)の問題
・ 例:エタンの完全燃焼反応

・ 格子エネルギーは電子親和力とイオン化エネルギーに注意!

格子エネルギーは、設問にそのまま出てもいいくらいよく見かけます。イオン化エネルギー(イオンになるために、電子を引き付けるために、必要なエネルギー)と、

電子親和力(原子が1価に陰イオンになる時に放出するエネルギー)は発熱なのか吸熱なのか間違えると計算結果をミスるので気を付けましょう。


エネルギーを求めさせる問題では、私は目で分かりケアレスミスを見つけやすいエネルギーの図を使ってました。方程式を差し引きするやり方は計算紙が汚くなりがちなので、ミスを起こさないようにしましょう
▶ 反応速度の問題

アレニウスの式については、受験会場ではほとんどの生徒が覚えていないし合格点を取るためにする勉強では必要ないです。ただ、式的に活性化エネルギーには比例しないなど簡易的なことは頭に入れておきましょう。

最後までお読みいただきありがとうございましたっ!SNSやブログなどで共有していただけると嬉しいです!


