国立大学2次試験2/25まであと
Resets every year at Feb 25 00:00 (JST).
この記事を読み終わると得られること
- 高校無機化学、無機化学の入試に出るポイント
- 典型金属元素、遷移元素

 編集者について
編集者について
河合全統記述模試にて、偏差値40台から英数物化を自力で70前半まで1年以内に伸ばしました。過去、数物化の勉強法を載せた記事がGoogle検索1位獲得。現在は暗号資産マーケットのDefi、金融取引を苦戦勉強中。
▶ 1族金属元素(アルカリ金属)
- 第六周期のCs(セシウム)まで炎色反応が起こる
- やわらかく、融点が低いので灯油中に保存
- 単体は金属結合が弱く結晶はすべて体心立方格子
- 水を還元させて水素を発生させる Na+H2O⇒NaOH+H2
- 周期が大きくなるほど、最外殻電子が中心から遠くなり原子半径が大きくなる。そのため、融点が下がる。e-を放出しやすくなりイオン化エネルギーが下がり、反応性が高まる
・ Na ナトリウム
・アンモニアソーダ法によるNa2CO3の製法
 十硬ノボラックちゃん
十硬ノボラックちゃん
炭酸ナトリウムは水によく溶けます。ガラスやセッケンに使われ、ソーダ灰ともいわれる
アンモニアソーダ法の概要図
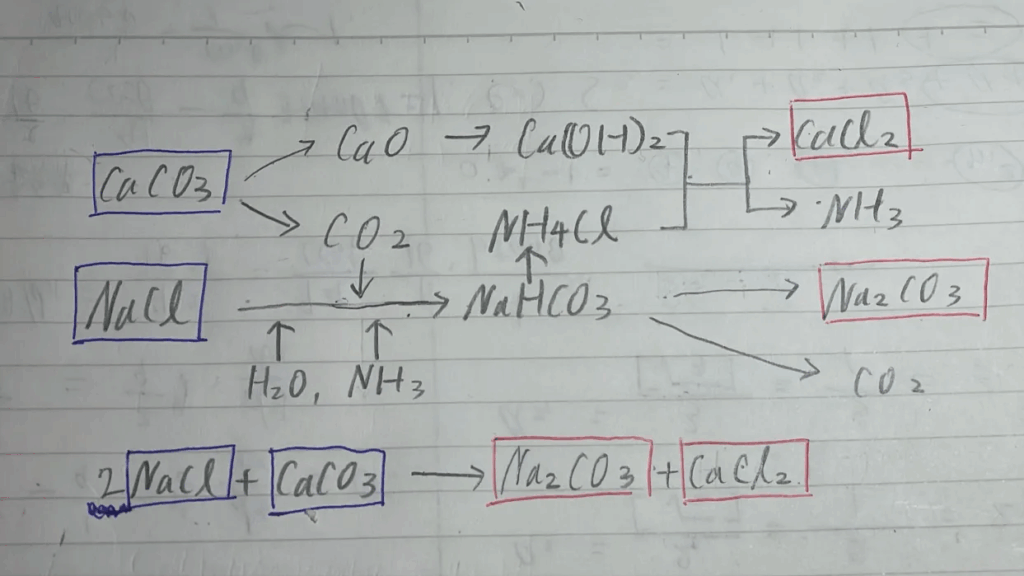
・NaHCO3の性質
 十硬ノボラックちゃん
十硬ノボラックちゃん
- 水溶性:酸性塩だが、水溶液は弱塩基を示す。HCO3-
- 2NaHCO3 → Na2CO3 + CO2 + H2O
▶ 2族金属元素(アルカリ土類金属)
- マグネシウムとベリリウムを除くアルカリ土類金属のSO4-塩、CO3-塩は水に難溶
- カルシウム・ストロンチウム・バリウムは、水によく溶け水酸化物を生成。強塩基を示す。(ストロンチウムは温度により溶解度が異なるが覚えなくていいかも)
- Raまで炎色反応
- アルカリ金属よりも価電子が1つ多く、それが自由電子になりアルカリ金属よりも金属結合が強くなる
- Beは常温の蒸気、Mgは高温の熱水と激しく反応。マグネシウムとベリリウムの水酸化物は水に溶けにくく弱塩基性を示します。
・ Ca カルシウム
・ セッコウから焼きセッコウ
 十硬ノボラックちゃん
十硬ノボラックちゃん
二水和物なのは、せっこうのせと、セカンド(2)のセが同じと覚えました。
・ さらし粉の生成
 十硬ノボラックちゃん
十硬ノボラックちゃん
しーえーしーえるし-えるおーえいちつーおーと詠唱しまくってたら覚えてました。
- Ca(OH)2 + Cl2 →CaCl・ClOH2O
- CaCl・ClO 2H2Oは高度さらし粉
・ Ca カルシウム関連
- CaCO3 →CaO + CO2 CaOは乾燥剤や発熱材に使用
- CaO + H2O →Ca(OH)2
- Ca(OH)2 + CO2 →CaCO3 +H2O
- CaCO3 + H2O + CO2 ⇄Ca(HCO3)2
- CaCO3 + 2HCl →CaCl2 +CO2 +H2O
当サイトのコンテンツはすべて無料で閲覧できます!以下の作業用勉強タイマーで読者の勉強時間を最大効率化させるお手伝いもできたら嬉しいです!

▶ 3~11族(遷移元素)
- 価電子数がほぼ一定のため、同じ周期の元素の化学的性質が似ている
- 典型金属元素に比べて、原子半径が小さく金属結合が大きいので融点が高く密度も大きい
- イオン、化合物では内側の電子殻が未閉殻なので可視光の吸収が起こり有色であることが多い。例えば鉄イオンやクロムイオン
・ Fe 鉄(体心立方格子)
 十硬ノボラックちゃん
十硬ノボラックちゃん
鋼(こう)の生成がよく出ます。1モルの三酸化二鉄からは最終的に2モルの銑鉄が得られます。
・ 一酸化炭素が還元剤となって三酸化二鉄から銑鉄を生成
- 3Fe2O3 + CO →2Fe3O4 + CO2
- Fe3O4 + CO →3FeO + CO2
- FeO + CO →Fe + CO2
- (全体の式)Fe2O3 + 3CO →2Fe + 3CO2
・ Fe2+の呈色
- Fe2+:淡緑色、Fe(OH)2:緑白色
- K3[Fe(CN)6]を加え、濃青色
・ Fe3+の呈色
- Fe3+:黄褐色
- Fe(OH)3:赤褐色
- K4[Fe(CN)6]を加え、濃青色
・ 鉄の酸化物
- FeO:天然には存在しない
- Fe2O3:赤鉄鉱として天然に存在
- Fe3O4:天然では磁鉄鉱として存在
・ Cu 銅(面心立方格子)
 十硬ノボラックちゃん
十硬ノボラックちゃん
11族はCu、Ag、Auと有名な金属元素が多いため、ポッキーどうぎんきんで覚えておくといいかも
・ 陽極泥まで考えるCuの電解精錬
Cuは天然では主に黄銅鉱(CuFeS2)として産出、空気と共に加熱酸化したのち粗銅になる。これを電気分解する
粗銅版は、Cu以外にもZn,Fe,Ni,Au,Agが含まれる。Cuよりもイオン化傾向が小さいAuやAgは陽極の下に泥として堆積します。
・ Cuの化合物
- CuO:黒色、1,000度以下で銅を空気酸化(加熱)、水酸化銅(Cu2O)を加熱脱水しても得られる
- Cu2O:赤色、銅を1,000度以上で加熱
- CuSO4・5H2O:無水物は無色の粉末。4分子のH2OがCu2+に配位結合、残りの1分子はSO42-と水素結合
・ Cr クロム(体心立方格子)
・ 酸化クロムと二クロム酸の色の推移
- CrO42-(黄色) + 2H+ →Cr2O72+(オレンジ) +H2O
- Cr2O72+(オレンジ) + 2OH- →CrO42- +H2O
・ 酸化還元
・ Mn マンガン
 十硬ノボラックちゃん
十硬ノボラックちゃん・ 酸化還元
- MnO4- + 8H+ +5e- → Mn2+ + 4H2O
- 酸性水溶液中でのKMnO4(過マンガン酸カリウム)反応
- MnO4- + 2H2O +3e- → MnO2 + 4OH-
- 水溶液が中性の場合
- MnO4- + e- → MnO42-
- 水溶液が塩基性の場合
・ H2O2の分解で触媒として利用
 十硬ノボラックちゃん
十硬ノボラックちゃん
1モルの過酸化水素から1モルの酸素と2モルの水が生成されます。
- H2O2 → O2 + 2H2O
- 過酸化水素をMnO2(二酸化マンガン)を触媒として酸素と水に分解
- H2O2 →2H2O + 2H+ + 2e-
- 過酸化水素が還元剤になる時と混同しないようにしましょう
・ Ag 銀(面心立方格子)
 十硬ノボラックちゃん
十硬ノボラックちゃん
銀は電気、熱を最もよく通します。電気・熱伝導性の順番は銀銅さんの家にはAuがあるで覚えました。
・ 原料は硝酸銀
銀はAgNO3の結晶が原料。性質として、感光性があり水によく溶けることを覚える
・ Ag+と少量の塩基で酸化銀の褐色沈殿
AgOHじゃなく、Ag2Oが沈殿します。本当によく出ます。
・ Ag2Oが褐色沈殿している溶液に多量のNH3水溶液
- [Ag(NH3)2]+:ジアンミン銀イオンが錯イオンとして溶けます
・ ハロゲン化銀
- H2O:AgFのみ溶解
- NH3:AgCl、AgBrのみ溶解
- AgCl、AgBr、AgIは配位能力の高いNa2S2O3とKCN水溶液に溶けて、それぞれ[Ag(S2O3)2]3-と[Ag(CN)2]-を作ります。
・ 銀鏡反応
- アンモニア性硝酸銀水溶液にアルデヒドを加えると1molのアルデヒドに対して2molのAgが析出します
- R-CHO + 2[Ag(NH3)2]+ + 3OH− → R-COO− + 4NH3 + 2H2O + 2Ag
・ TiとW チタンとタングステン
 十硬ノボラックちゃん
十硬ノボラックちゃん
そんなに両方とも出ない印象だけど覚えておきましょう。
- TiO2:光により、表面にある水が酸化され、有機物からe-を奪い酸化させるので抗菌作用を発揮。化粧品、建物の外壁、空気清浄フィルターに使用
- W:融点が3,400度と高く、フィラメントに使われる
▶ 1・2族以外の典型金属元素
▶ 12族
・ Al アルミニウム
 十硬ノボラックちゃん
十硬ノボラックちゃん・ 両性金属元素なので水に溶け水素発生
- 2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2
・ Al2O3を生成するテルミット反応
- 2Al + Fe2O3 → Al2O3 + 2Fe
・ Al2O3を生成するバイヤー法
- Al2O3 + 2NaOH + 3H2O → 2Na[Al(OH)4]
- Na[Al(OH)4]を水に→ Al(OH)3 + NaOH
- 2Al(OH)3 → Al2O3 + 3H2O
・ Alを得るホール・エルー法
 十硬ノボラックちゃん
十硬ノボラックちゃん
融解した氷晶石(Na3AlF6)とAl2O3を電気分解。
難関大のどっかで氷晶石(Na3AlF6)の化学式を覚えておいたのが過去問で助かった記憶があるのですが忘れましたw NASAアルファシックスとかで宇宙のNASAと冷たい=氷晶石の氷の漢字を結び付けて覚えてました。
- 陰極:Al3+ + 3e- → Al
- 正極:C + 2O2- → CO2 + 4e-
- 正極:C + O2- → CO + 2e-
・ ミョウバン
 十硬ノボラックちゃん
十硬ノボラックちゃん
AlK(SO4)3とK2SO4の混合溶液濃縮したもので水中電離する
- AlK(SO4)2・12H2O → Al3+ + K+ + 2SO42- + 12H2O
▶ 13族
・ Sn スズ
 十硬ノボラックちゃん
十硬ノボラックちゃん
酸化数0、+2、+4を取ります。
鉄のメッキや有機分野の酸化還元でよく出るイメージ
- おもちゃなど、鉄の上にSnをコーディングします。Feよりもイオン化傾向が小さく、水に触れても丈夫です。ですが、傷がつくと、Feの方がイオン化傾向が大きいので以下のイオン反応式が起こります。
- 鉄へのメッキ:Fe → Fe2+ + 2e-
- 鉄へのメッキ:O2 + 2H2O + 4e- → 4OH-
- 還元剤:Sn → Sn4+ + 4e-
- 酸化剤:ニトロベンゼン→アニリン
・ Pb 鉛
 十硬ノボラックちゃん
十硬ノボラックちゃん
鉛と同じく、酸化数0、+2、+4を取ります。鉛蓄電池は超頻出。
- 負極:Pb + SO42- → PbSO4 + 2e-
- 正極:PbO2 + 4H+ SO42- + 2e- → PbSO4 + 2H2O
- 一言メモ:この鉛蓄電池を題材にする問題はかなり出るので、係数を覚えてもいいかもしれません。
▶ 塩酸・炭酸・シュウ酸・硫酸・クロム酸イオンによる金属沈殿
| 水溶液 | 沈殿する金属 | 語呂合わせ |
|---|
| 塩酸 | Pb,Ag | 銀ナマを円に換える |
| 炭酸 | Ba,Sr,Ca | ばかにする炭酸 |
| シュウ酸 | Ba,Sr,Ca | ばかにするシュウ酸 |
| 硫酸 | Ba,Sr,Ca,Pb | 硫酸を馬鹿にするな |
| CrO4(2-) | Ba,Pb,Ag | バナナを銀貨で買って苦労する |
▶ 合金暗記:語呂合わせ
 十硬ノボラックちゃん
十硬ノボラックちゃん
金属元素を推定させる問題で、「航空機やアタッシュケースに使われる合金に含まれるもの」などと遠回しに問われます。合金の名前を覚えるぞ!というより(もちろん名前は覚える!)は、用途と構成元素を抑えて語呂合わせで覚えるのが速攻で知識を引き出せるので良いです。
合金の名前を答えるだけで点数が降ってくる問題もあるので、抑えておきたい。
| 合金の名前と元素構成、用途 | 語呂合わせ |
|---|
| Cu 銅関連 | ・Snが含まれると青銅
・Znが含まれると黄銅
・Niが含まれると白銅 | 青春のキズは白紙に
青銅とSnで青春
黄銅とZnでキズ
白銅とNiで白紙
ちょっと悲しい語呂合わせ、、、 |
| Al アルミニウム関連 | ・ジュラルミン AlにCuとMg
→航空機やアタッシュケースに使用
・アルマイト Alの表面に厚い酸化被膜
・ルビー Al2O3にCrが含有
・サファイア Al2O3にFeとTiが含有
| ジュラルミン:AI民曲がるのどう?
クルル:Crとルビーのル
サファイアフェチ:FeTiをフェチと読みました |
| Fe 鉄 | ・ステンレス鋼 FeにCrとNi | ステンレスに黒って:
Crを黒、てをFeにしました |
| Ni+Cr ニッケルとクロム | ・ニクロム | ニクロム
二:ニッケル
クロム:そのままクロム |
| Pb 鉛 | ・Snが含まれるとはんだ | |
| Hg | ・アマルガム 水銀が50%、あとは銀、スズ、銅など
→虫歯治療で使う銀色の詰め物 | |
▶ 【東大生の思考を盗む】東大・京大・科学大・一橋後期・医学部医学科・早慶理工学部を本気で狙う方へ
このサイトでは、入塾を受け付けている数々の塾の中から本当に難関大受験生向けだなと感じた個別指導塾を選んでいます。本質を見抜く力と時間効率を極めた東大生に学ぶ時間は、受験科目や難易度の違う他の大学の生徒からは得られません。
もし 「独学で限界を感じている」「効率を最大化したい」と思ったら、東大生・プロ講師による個別指導塾の無料相談が利用できます↓
- 当サイトに掲載している情報は、読者が偏差値70を必ず達成できることを保証するものではないです。必ず、自身の教科書と参考書を熟読し、参考程度にしてください。
- ぜひ授業や学校の定期試験、塾講師バイト時の参考にしたいものがあれば印刷したりして使って下さい!出典元のリンクをSNSや公式サイトへリンクしてもらえるとかなり嬉しいです!!お願いします!
- このページに掲載している情報は、AIによって正確性を検査してもらった上で公開しています。万が一誤りを見つけた場合は以下の二点をコメント欄にてお教えください。①誤っている箇所の文や式、②正しいもの
- 出典:理系大学受験 偏差値70への道
- リンク:https://rikei-tokyo.com
当サイトはすべての理系大学受験生を心から応援しています。頑張れ!
 グルフル転化糖ちゃん
グルフル転化糖ちゃん
最後までお読みいただきありがとうございましたっ!SNSやブログなどで共有していただけると嬉しいです!
























