高校無機化学:ハロゲンと希ガス以外の非金属元素/よく出るものまとめ【偏差値70超えの暗記ノート】
国立大学2次試験2/25まであと
0
DAYS
:
00
HRS
00
MIN
00
SEC
Resets every year at Feb 25 00:00 (JST).


河合全統記述模試にて、偏差値40台から英数物化を自力で70前半まで1年以内に伸ばしました。過去、数物化の勉強法を載せた記事がGoogle検索1位獲得。現在は暗号資産マーケットのDefi、金融取引を苦戦勉強中。
▶ 14族
・ Si ケイ素

Si(ケイ素)は自然界には存在せず、単体が欲しいときは二酸化ケイ素から取り出します。

シリカゲルにするまでの工程がよく出題されます。
▶ 15族
・ P リン

同素体は、同一元素の単体のうち原子配列や結合様式の関係が異なるものです。
・リンの同素体
| 黄リン | 赤リン | |
|---|---|---|
| 式 | P4 | P(組成式) |
| 融点 | 110度くらい | 110度くらい。斜方硫黄よりちょい高め |
| 毒性 | 猛毒 | 毒性が少ない |
| CS2 | 溶ける | 溶けない |

当サイトのコンテンツはすべて無料で閲覧できます!以下の作業用勉強タイマーで読者の勉強時間を最大効率化させるお手伝いもできたら嬉しいです!

▶ 16族
・ S イオウ
・硫黄の同素体

大事なことなのでもう一回!同素体は、同一元素の単体のうち原子配列や結合様式の関係が異なるものです。
| 斜方硫黄 | 単斜硫黄 | ゴム状硫黄 | |
|---|---|---|---|
| 式 | S8 | S8 | S(組成式) |
| 融点 | 110度くらい | 110度くらい。斜方硫黄よりちょい高め | |
| 特徴 | 常温で安定(よく出ます) | 針状の結晶(単純な針と暗記) | 少し弾性力がある |
・接触法

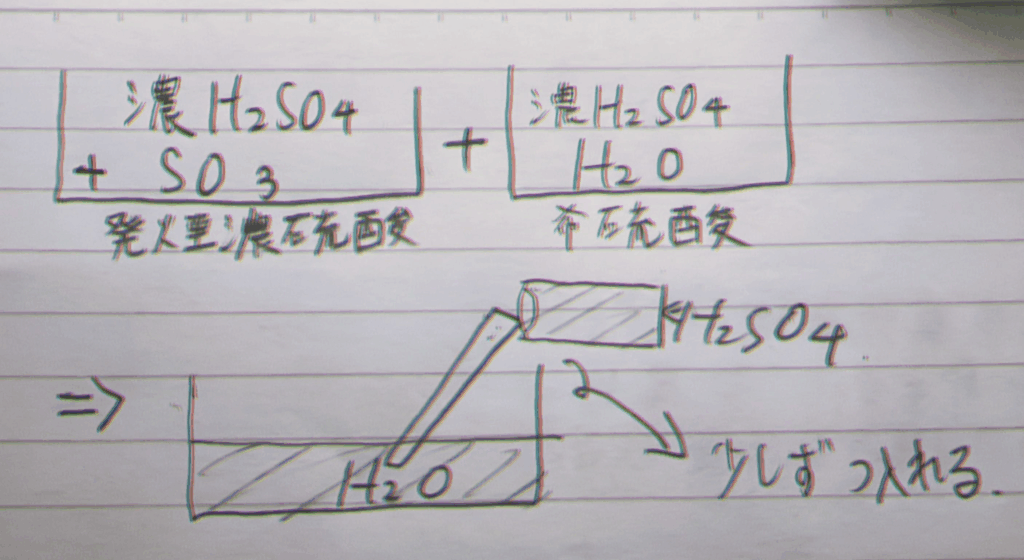
「接触法の名前自体」「なぜ水に硫酸を少しずつ入れるのか」「硫化鉄を酸化して二酸化硫黄を得る式」あたりが問われるイメージです。

三酸化硫黄SO3は、水と激しく作用して濃硫酸が飛び散り危険です。そのため、濃硫酸を作る時は下の2つを混ぜてります。
▶ 【東大生の思考を盗む】東大・京大・科学大・一橋後期・医学部医学科・早慶理工学部を本気で狙う方へ
このサイトでは、入塾を受け付けている数々の塾の中から本当に難関大受験生向けだなと感じた個別指導塾を選んでいます。本質を見抜く力と時間効率を極めた東大生に学ぶ時間は、受験科目や難易度の違う他の大学の生徒からは得られません。
もし 「独学で限界を感じている」「効率を最大化したい」と思ったら、東大生・プロ講師による個別指導塾の無料相談が利用できます↓


